Лилия Зиганшина: «Big Pharma заявляет, что разработка одного наименования лекарства обходится в $1 миллиард»

Считается, что именно талидомидовая трагедия послужила мощным толчком к созданию концепции основных лекарств и специальности «клиническая фармакология» — катастрофа со всей наглядностью и очевидностью показала, что коротких исследований на доклиническом и клиническом этапах испытаний явно недостаточно для того, чтобы лекарство было выпущено на рынок. Однако, даже несмотря на этот печальный урок, Big Pharma продолжает противостоять концепции Основных лекарственных средств. Подробнее в интервью «Реальному времени» Лилии Зиганшиной, заведующей кафедрой фундаментальной и клинической фармакологии Института фундаментальной медицины и биологии КФУ.
«К настоящему времени Основных лекарств не больше 400»
— Лилия Евгеньевна, что такое Основные лекарства и концепция Основных лекарственных средств?
— Это лекарственные средства, обеспечивающие потребности здоровья подавляющего большинства населения доказанным образом. Концепция Основных лекарственных средств была предложена ВОЗ в 70-е годы прошлого века, когда мы еще жили за железным занавесом. Уже тогда лекарств было очень много, и практикующему врачу на что-то надо было опираться при выборе медикаментов для лечения пациентов. Причем если не большая, то значительная часть этих лекарств была из так называемой категории «Me too» — «мы тоже». Иными словами, это многочисленные разновидности и аналоги уже имеющихся и испытанных лекарственных средств. Примерно в это же время, с разницей буквально в один год, экспертное сообщество ВОЗ выходит с инициативой ввести в медицинскую классификацию специальность «врач-клинический фармаколог».
— Их много — Основных лекарственных средств?
— В 1977 году был принят список из 186 наименований. В версии 2005 года их было уже 315. К настоящему времени их не больше 400. Эффективность и безопасность основных лекарств доказана практикой мирового здравоохранения. Также доказано, что так называемые страны третьего мира, или, по классификации Всемирного банка, страны с низким уровнем дохода, в гораздо большей степени защищены от лекарственных катастроф, чем развитые страны. Вехой в распространении концепции Основных лекарств считается публикация 2004 года профессоров Ганса Хогерзайла и Ричарда Ленга о том, что богатые страны, где работает Big Pharma, должны наконец извлечь уроки из концепции Основных лекарств. Между тем, по понятным причинам, именно Big Pharma, делает постоянные и настойчивые попытки подвергнуть концепцию ревизии, протолкнуть туда свои продукты, внедряя в широкие академические круги мысль о том, что концепция — это для самых отсталых стран, но не для «цивилизованного» человечества. Хотя, повторюсь, список Основных лекарств ежегодно утверждается крупнейшим медицинским сообществом планеты — Всемирной организацией здравоохранения.
— Почему Big Pharma так не заинтересована в развитии концепции?
— Потому что следование ей вредит финансовым интересам фармацевтических корпораций. Big Pharma со всех трибун заявляет, что разработка одного наименования лекарственного средства — от скрининга молекулы до вывода препарата на рынок — обходится ей в миллиард долларов. Однако это даже не лукавство, а откровенный обман: львиную долю выручки Big Pharma снимает с препаратов из категории «Me too», а львиную долю стоимости лекарства, которую за него платят пациенты, составляют затраты не на научные разработки, а на рекламу. Причем не только на прямую рекламу, а на проведение конференций, на работу полчищ медицинских представителей (сейчас их называют консультантами). Кстати, на Западе люди с медицинским образованием давно уже в торговле не работают — это торговые представители (sales representatives), основная и единственная функция которых – продать и т. д. Используются все каналы — подарки, письма, «подсовываются» красивые презентации, с которыми надо выступить на «научной» конференции и т. д., и все это фармкомпаниями оплачивается. И чем выше статус ученого и врача, тем выше оплата.
Ужасно, что производители лекарственных средств в прямой рекламе своей продукции беззастенчиво используют логотип ВОЗ, хотя в уставе организации политика использования логотипа, как любого другого зарегистрированного знака, прописана совершенно четко: использовать его можно только с разрешения ВОЗ. Организация, конечно, пытается это как-то отслеживать, но каждого за руку, увы, не поймаешь.
«Треть затрат Big Pharma в продвижение своей продукции — это вознаграждение торговым представителям»
— А вы располагаете данными, какие средства в рекламу и продвижение препаратов вкладывает Big Pharma?
— У меня есть данные за 2004 год, и за это время если что-то и изменилось, то только в большую сторону. Так вот, по итогам 2004 года только в США в рекламу и продвижение медикаментов производителями было вложено 57,5 млрд долларов. Примерно четверть этой суммы пришлась на немониторируемое (то есть специально не отслеживаемое) продвижение, по одной трети — вознаграждение торговым представителям и прямая реклама потребителям, и остальное — другие каналы продвижения, в том числе через профессиональные медицинские и научные журналы.
— Лилия Евгеньевна, если взять обычную среднестатистическую аптеку, можете ли вы сказать, какая часть продаваемых препаратов будет из списка Основных лекарств?
— Я не ошибусь, если скажу, что неосновных лекарств в десятки раз больше. Такие исследования на государственном уровне, к сожалению, не проводятся. Мы силами магистрантов, аспирантов, соискателей проводили подобное исследование, по результатам которого пришли к выводу, что надо еще очень много работать, чтобы привести действующие на территории РТ и РФ регуляторные списки хотя бы в приблизительное соответствие с моделью лекарственного обеспечения, принятой ВОЗ.
В 2006 году по заказу Минздрава был проведен анализ, какие лекарства закупались через Фонд обязательного медицинского страхования для льготного и бесплатного обеспечения медикаментами. По результатам исследования стало ясно, что львиная доля огромных государственных денег шла компаниям-производителям необоснованно. К примеру, самым закупаемым средством был предуктал — препарат для сердечников, который никак не влияет ни на продолжительность жизни, ни на шансы испытать острый коронарный синдром. То исследование было первым и, к сожалению, единственным; даже если подобная работа и проводилась в дальнейшем, то результатов в открытом доступе не было.
— Но какие-то выводы сделаны были?
— Я думаю, что «Фарма-2020» принималась все-таки с учетом этой аналитики. Во всяком случае, в документе сделана установка на отечественное производство, на использование генерических средств с максимально доказанной эффективностью и годами проверенной безопасностью. Другой вопрос, что даже в уже принятую стратегию все так же пытаются залезть и ревизовать ее фармацевтические корпорации.
«Новая молекула рождается в лабораториях университетов. Big Pharma лишь осуществляет дальнейшее внедрение»
— Два года назад Казанский университет присоединился к международной студенческой организации UAEM, объединяющей университеты, ратующие за предоставление доступа к Основным лекарствам. Насколько эта организация имеет вес в научной и медицинской среде?
— Полное название организации — «Университеты, объединившиеся за доступ к основным лекарствам», и она признана во всем мире. Началось все в 2001 году, когда студенты Йельского университета (США) обнаружили, что лекарство для лечения ВИЧ/СПИДа, разработанное в лаборатории их университета, было коммерционализировано, причем настолько «успешно», что сделало его недоступным для применения подавляющим большинством больных ВИЧ/СПИДом. Студенты выступили за разрешение производства генерических версий этого лекарства (ставудина), что позволило снизить цены более чем в 30 раз. Сегодня UAEM объединяет более 120 университетов по всему миру. Наши студенты благодаря сотрудничеству с Всемирной организацией здравоохранения и участию в Кокрейновском сотрудничестве уже участвовали в нескольких крупных международных форумах, посвященных проблеме доступа к Основным лекарствам.
— А какая часть лекарственных средств создается в университетах, и какая — в лабораториях Big Pharma?
— Скажем, вклад университетских лабораторий в создание новых лекарственных средств принципиален — именно там рождается сама новая молекула. Однако дальнейшее внедрение осуществляет Big Pharma, которая и устанавливает неадекватные цены на «свои» лекарства, ссылаясь на дороговизну разработки, испытаний и вывода на рынок. Вот вам только один пример. В 2015 году в Женеве проходил Социальный форум ООН «Доступ к лекарствам в контексте прав человека на здоровье». В докладе содиректора организации «За мир, свободный от СПИДа» Стивена Льюиса звучали следующие цифры: «Компании назначают цену в десятки тысяч долларов за курс препаратов, себестоимость которых составляет всего около 100 долларов, при этом сами компании агитируют правительства стран за сохранение такого статус-кво».
— Клинические исследования, в которых задействованы врачи, многие из которых считаются светилами в своей области, — это тоже часть рекламных компаний корпораций, представляющих Big Pharma?
— В значительной степени… И зачастую эти исследования оказываются просто ненужными — это тот же инструмент продвижения, та же реклама: специалисты, которые ведут такие исследования, получают хорошее вознаграждение, несравнимое с зарплатой профессорско-преподавательского состава. За право проводить такие исследования ведется нешуточная конкуренция, и оно доверяется лишь тем, кто покажет результаты, в которых заинтересованы фармкомпании. Науке здесь места не остается. Так что сами понимаете, насколько результаты таких исследований являются объективными. Даже так называемые рандомизированные исследования, когда одни участники получают испытуемое лекарство, а другие плацебо, не дают гарантии полной безопасности пациента: есть множество факторов, способных исказить картину исследования, причем факторы эти накладываются один на другой.
Львиная доля сведений о безопасности или небезопасности лекарственных средств была получена человечеством не в ходе испытаний, а из многолетних клинических наблюдений. Формуляры ВОЗ, в которых публикуются перечни Основных лекарств, составляются в том числе на основе спонтанных сообщений врачей, пациентов, есть специалисты, которые эти сообщения отслеживают и оценивают на предмет наличия в них причинно-следственной связи. Это очень серьезный раздел клинической фармакологии, который в своем развитии сталкивается с множеством препятствий административного, культурологического и финансового характера. Сегодня ВОЗ поддерживает специальную базу таких спонтанных сообщений. Есть даже ученые, которые анализируют блоги и форумы, например, форумы мамочек, которые, как известно, весьма активны в обсуждении здоровья своих детей. И сейчас весь мир работает над созданием интеллектуальных семантических систем, способных проанализировать весь этот огромный массив неупорядоченной информации, которую отследить, увидеть в ходе клинических испытаний невозможно.
— Сегодня покупка лекарств стала сродни приобретению базовых продуктов питания: часто и в больших объемах. Можно ли переломить эту ситуацию и что делать нам, простым потребителям, чтобы не стать жертвой рекламы лекарственных средств?
— Ответить на этот вопрос я хочу выражением Бориса Евгеньевича Вотчала, отца отечественной клинической фармакологии: «Базовый принцип — поменьше лекарств: только самое необходимое». Эти слова были сказаны им в 1965 году в актовой речи, и к настоящему времени их актуальность, как видим, только возросла.
Цена такова, какова она есть!
Как бывает обидно, когда вы потратили свое время и энергию, консультируя посетителя аптеки, презентуя препарат, отвечая на все его вопросы и возражения, а в результате вам говорят: «Я лучше пойду и посмотрю в другой аптеке». А если таких покупателей 10—20 и больше в день? Сколько денег при этом теряется? Сколько сил расходуется понапрасну? Почему же люди не покупают у вас и в вашей аптеке? На основании того, что они стали более требовательными и капризными, разборчивыми или по какой-то другой причине? Или, может быть, потому, что по соседству с вашей аптекой находятся еще пять конкурентов? Как удержать посетителей аптеки и сделать так, чтобы они регулярно совершали покупки именно в вашей аптеке?
Цена препарата
Спросите у любого первостольника, почему люди не покупают лекарственные средства — и моментально получите такие ответы на этот вопрос: «Не покупают, потому что у них просто нет денег на это», «Лекарства стали очень дорогими», «Цены на препараты повышаются каждый день».
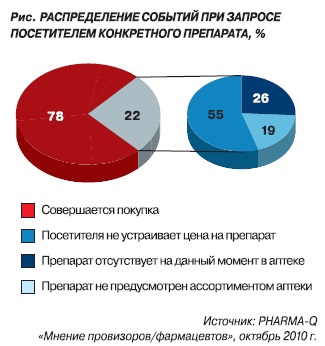
По мнению респондентов первого стола, принявших участие в исследовании PHARMA-Q, проводимом компанией Synovate Comcon, приобретение лекарственного средства происходит примерно в 4 из 5 запросов посетителей аптеки (78%). Причина более половины (55%) несовершенных покупок в том, что человека не устраивает цена препарата (рис.).
По определению, данному в Википедии, «цена — количество денег, в обмен на которые продавец готов передать (продать) единицу товара». С другой стороны, цена или стоимость — понятие абстрактное и определяется тем, насколько этот товар нужен покупателю, насколько он его сам оценивает. Какое лекарство является дорогим — то, которое стоит 500 или 5000 руб.? «Все зависит от обстоятельств и ситуации», — ответите вы и будете совершенно правы. В жизни случаются непредвиденные критические ситуации, допустим, когда серьезно заболел ребенок или близкий человек. Будет ли тогда стоять вопрос о цене? Готовы ли вы заплатить любую сумму за лекарственные средства или операцию, продав последнее, что есть, лишь бы родной вам человек выздоровел, или подумаете о том, как сэкономить и купить лекарство подешевле?
Почему лекарство стоит столько, сколько стоит
Как вы считаете, почему цена препарата 500, а не 100 руб. или 1200, а не 400? Часто бывает и так, что сами провизоры и фармацевты не понимают, из чего складывается стоимость. Это порой служит причиной неуверенности и нетвердости при ответе на так часто встречающийся вопрос посетителя или покупателя аптеки: «А почему так дорого?» Многие первостольники сами искренне считают, что некоторые препараты являются дорогостоящими, и дают совет покупателям приобрести более дешевое лекарство.
Процесс появления препарата на рынке — невероятно дорогостоящий, трудоемкий, многоэтапный и очень долгий по времени. В среднем на разработку нового лекарственного препарата, от стадии его разработки до регистрации, необходимо затратить 12—15 лет. Это также является и достаточно рискованным предприятием для компании-производителя, т.к. огромная научно-исследовательская работа, проделанная в течение нескольких лет, не гарантирует того, что новое лекарственное средство будет создано. Из 100 молекул до создания препарата доходят только 10—15. В реальную клиническую практику внедряется лишь один препарат из 5—10 тыс. стартовавших (по данным Американской ассоциации разработчиков и производителей лекарственных средств).
Общие затраты, начиная от поиска оригинальной молекулы до вывода препарата на рынок, составляют сегодня более 800 тыс. долл. США, и они непрерывно возрастают. В 1970-х гг. для вывода оригинального препарата на рынок требовалось 138 млн долл., в настоящее время — 800 млн долл. Именно этот факт и определяет то, что только очень небольшое количество крупных фармацевтических компаний в мире занимаются разработкой и созданием новых лекарственных препаратов. Современная тенденция фармацевтического рынка заключается в том, что многие компании-производители начинают объединяться, чтобы совместными усилиями покрывать колоссальные расходы на поисковые научные исследования, клинические испытания и внедрение препарата на рынок.
Основные этапы создания препарата (на примере отечественной компании)
Идея
Начало пути — это идея, гипотеза о новом препарате, базирующаяся на новых вдохновляющих или необъяснимых наблюдениях. Источниками идей могут служить научные данные и публикации, университетские исследования, научное сотрудничество, патентная литература, международные симпозиумы и исследования в собственных лабораториях.
Предпроект
Небольшая команда проверяет гипотезу при помощи биохимических методов и/или испытаний на животных. Если эксперимент имеет положительный результат и основное действующее вещество выявлено, запускается официальное исследование.
Продолжительность: около 1 года.
Исследование
Группа ученых начинает работу с основным действующим веществом, описывает его и устанавливает способ его производства. В рамках этой работы с целью определения действия препарата создаются экспериментальные животные модели с заболеванием, максимально приближенным к человеческому.
Продолжительность: интенсивная деятельность вплоть до начала доклинических исследований; затем постоянное научное сопровождение.
Производство
На этом этапе идет разработка аналитических методов и технологии производства действующего вещества и самого препарата. Начинается производство для доклинических и клинических исследований. Выработка препарата непрерывно растет на фоне повышения требований к его качеству. Продукт должен быть готов к полномасштабному производству к началу фазы III клинических исследований.
Продолжительность: 7—10 лет, на всем пути разработки.
Доклинические исследования
Чтобы убедиться в безопасности нового препарата для людей, ученые сначала испытывают его на животных, исследуют фармакологическое и токсическое действие препарата на все системы органов. В это время другая группа ученых подтверждает медицинскую гипотезу с помощью тестов на образцах тканей и крови человека и готовится к клиническим исследованиям. Этот этап часто знаменует переход от испытания к разработке.
Продолжительность: интенсивная деятельность в течение 1 года перед клиническими испытаниями, длится вплоть до регистрации препарата.
Клинические исследования
Когда безопасность и эффективность препарата доказаны на животных, начинаются исследования на людях. Компания проводит клинические исследования более чем в 50 странах с участием 15—20 тыс. человек ежегодно. После успешного завершения фазы 3 исследований следует подача документов на регистрацию препарата в соответствующие регуляторные органы.
Продолжительность: 5—7 лет.
Регистрация препарата
После того как эффективность и безопасность препарата подтверждены в ходе клинических исследований фазы 3, он должен получить одобрение регистрирующих органов в каждой отдельной стране перед выпуском на рынок. Все данные, полученные в период разработки, передаются в соответствующие инстанции в США (FDA), Европе (EMEA), Японии (PMDA) и в других странах, где требуется получение одобрения национальных регуляторных служб.
Продолжительность: 1—1,5 года.
Подготовка к выводу на рынок
Служба маркетинга участвует в процессе создания нового препарата, начиная с фазы 1 исследований или раньше, с целью изучения потребностей рынка в его разработке. Данный процесс включает подготовительную работу как внутри компании, между ее филиалами, так и за ее пределами. Результаты исследований озвучиваются на международных симпозиумах, наращивается информационная работа в медицинском сообществе.
Продолжительность: 7—10 лет до вывода препарата на рынок; деятельность наращивается по мере приближения запуска.
Вывод на рынок
В преддверии вывода препарата на рынок начинается масштабная кампания по организации сбыта. Определяется очередность запуска препарата в разных странах, согласуются цены на внутренних рынках, маркетинговые планы, объемы первых партий и т.д. Партии препарата готовятся к отправке. После получения одобрения первые заказы отправляются в филиалы, которые затем организуют доставку препарата до местных аптек.
Продолжительность: 6—12 месяцев до запуска.
Исследования фазы IV
Эти клинические и постмаркетинговые наблюдательные исследования начинаются после запуска лекарственного препарата с целью выявления возможных долгосрочных побочных эффектов, новых показаний к применению, сбора опытных данных по применению или особым факторам безопасности.
Продолжительность: зависит от масштабов, но может составлять 2—5 лет.
Объяснять покупателю в деталях об этой основной и важной составляющей стоимости лекарственного средства совсем не обязательно. Важно обладать этими знаниями, чтобы на вопрос посетителя аптеки: «А почему так дорого?» — твердо, уверенно и убежденно ответить: «А вы знаете о том, что компания-производитель потратила 1 млрд долл. и 10 лет для создания этого оригинального, эффективного и безопасного препарата?!»
Люди во всем мире и во все времена жаловались на цены. Как мудро сказал по этому поводу французский философ Поль Мишель Фуко: «Нет справедливой цены. Дешевизна не более и не менее точна, чем дороговизна». Правильной цены нет, но зато у вас есть профессиональное объяснение того, из каких факторов складывается стоимость. Остается лишь правильно донести эту информацию до потребителя. И не стоит огорчаться, если покупка все же не состоялась: в любом случае ваш профессиональный авторитет получил дополнительные баллы доверия
Корпоративные инновации: как выводить на рынок новые продукты?
Традиционно на рынке существует две основные модели развития новых технологий и продуктов: разработка внутри компании и покупка готовых решений с рынка. Последний путь, так называемые открытые инновации, в нашей отрасли не применим — здесь не у кого и нечего покупать. Даже если что-то все-таки находится, то, как правило, разработки очень далеки от рынка.
Где искать идеи?
Как искать идеи для новых продуктов? Смотрите на конкурентов! В нашей компании мы обычно берем лидеров рынка той или иной продукции, тщательно их изучаем. Отправляем их товары в лабораторию, выясняем, что, как и почему они делают, куда и что добавляют.
Так мы поступили при изготовлении нашей медицинской маски премиум-класса под брендом Latio. Ориентировались мы на мирового лидера в этой области, компанию Kimberly Clark. Первоначальная задача — создать продукт, не уступающий им по качеству и функционалу. Взяли их маску за основу, а когда углублялись и разрабатывали собственный проект, дополнительно внесли изменения и уже с учетом этих корректировок подбирали оборудование. Например, мы добавили фиксатор формы: это специальная пластмассовая полоса по всей длине, которая не дает маске соприкасаться с ротовой полостью. Таким образом, маска не намокает, идет более комфортное дыхание, более эффективная фильтрация.
Идеи улучшений обычно рождаются из повседневного опыта: если ты глубоко изучаешь какую-то тему, постоянно думаешь о продукте, его функционале, сам используешь его, в конце концов к тебе приходит правильное решение.
Еще один источник «продуктового вдохновения» — посещение специализированных, особенно зарубежных, выставок. Там можно найти самые неожиданные решения других стран в вашей или смежной сфере. Например, на одной из выставок мы увидели японские маски для детей с широкой (1 см) ушной резинкой.Почему бы не сделать такой же продукт в России? Маленькая резинка обычно давит на уши, а у ребенка ушки совсем нежные, и чтобы ему было комфортно, можно сделать маску с широкой резинкой.
С одной из международных выставок мы привезли идею делать детские подгузники очень высокого качества. В данном случае ориентировались опять же на японцев с точки зрения качества, мягкости и легкости их продукта. Сейчас эти свойства будем воплощать и в нашем продукте. Буквально через пару месяцев уже планируем выйти на рынок, производство практически запущено, ждем упаковку и утрясаем прочие мелкие рабочие процессы. Здесь мы пробуем новую для себя схему — выводим на рынок сразу продукт премиум-класса.
Итак, нашли идею, сформулировали видение продукта, что дальше? Включается наше русское «А почему бы не сделать лучше?». И мы начинаем смотреть, изучать, что можно добавить, что исправить, чтобы обогнать всех? По каждому продукту у нас есть проектный менеджер, который занимается развитием технологических проектов. Его задача — постоянно что-то улучшать: упаковку, качество, функционал.
Сколько времени занимает разработка продукта?
Срок реализации производственной идеи разный — от года до 3-х лет. Здесь все сильно зависит от загруженности директора и команды, которая занимается проектными работами. Если мы будем погружены только в этот проект, то на составление предварительного бизнес-плана может уйти два-три месяца. Еще столько же надо закладывать на выбор оборудования: нужно будет ездить в разные страны, посещать похожие заводы. Итого — примерно полгода до подписания инвестиционного проекта и запуска, который, к слову, тоже может сильно разниться по срокам. Нужно ли искать инвестиции или деньги уже есть? Если проект — это оборудование, как правило, его изготовление, установка, отладка, пуск занимают еще от 4-х до 12-ти месяцев.
Как мотивировать команду заниматься инновациями?
Сотрудников мы мотивируем деньгами. Ставится задача, и когда уже есть понимание, куда мы двигаемся, назначается бонус за выполнение данной задачи. Сотрудник должен самостоятельно составить список своих тактических и стратегических целей, утвердить их и выполнить.Чем больше у него задач, тем больше возможностей получить дополнительные деньги. Как правило, в разработке продукта принимает участие целая команда специалистов. Для отдела продаж, соответственно, ставятся задачи по разработке интересного продвижения и рекламы, чтобы с минимальными бюджетами получить максимальный результат.
Сколько стоит разработка?
Дать среднюю оценку стоимости создания и вывода на рынок нового продукта сложно, все зависит от масштабности проекта. У нас есть небольшие инновации, мы называем их тактическими, их можно внедрить за короткий период времени. Постоянная часть расходов — содержание отдела разработки. У нас есть команда, которая системно занимается инновациями: один бизнес-план написали, утвердили, делают следующий, пока мы, например, ищем деньги. Деньги нашли — они начинают его реализовывать. Поэтому у нас есть отдел, который стоит порядка 200 000 руб. в месяц, это отдел, работающий на будущее компании.
Вторая часть расходов — затраты на командировки, закупки образцов. Когда мы создавали наш первый продукт, я ездил на неделю в Китай — это уже 300 000.
Обычно на разработку проекта уходит минимум миллион. А вот реализация может стоить от 1 до 100 млн руб.
Мы, например, только на первой стадии потратили на запуск производства медицинских масок более 20 млн руб., позже еще вкладывались на второй и дальнейших стадиях. И это цифры с учетом постепенной закупки оборудования: сначала один станок купили, загрузили, потом второй, третий и т.д.
Как долго окупается новый продукт?
По моему опыту, средний срок окупаемости нового продукта — пять лет. Первый проект всегда окупается дольше, чем последующие. У меня даже были проекты, где мы выходили в ноль всего за год. В основном это касается улучшающих инноваций: например, мы производим резинки на маски, спрос на продукт уже сформирован. А есть у нас производство европейской маски — там окупаемость составит до 10 лет.
Как вывести новый продукт на рынок?
Самая большая ошибка — думать, что ваш суперинновационный продукт кому-нибудь нужен. Если вы делаете прорывную инновацию, значит, рынка для нее еще нет. А если нет рынка под этот продукт, то кому вы планируете его продавать? Это тупик.
Как правило, чистые инновации — это очень тяжелая вещь. Формировать рынок под инновацию, как правило, могут только крупные компании, которые уже давно в отрасли и обладают определенной финансовой прочностью.
Я инновации всегда соединяю с обычной продукцией, благодаря которой выхожу на рынок, завоевываю доверие потребителей, а потом им уже предлагаю: «А попробуйте еще и вот этот новый продукт». Это более легкий способ продвижения инноваций.
Когда мы только запускали компанию, выходили на рынок со стандартным продуктом: делали обычную маску, нарабатывали себе клиентов. Люди не понимали, зачем покупать маску за десять рублей, если есть за рубль? В чем разница, почему такая цена? В первую очередь, так говорили дистрибьюторы, которые не умели работать с премиум-сегментом и потому считали, что покупателю не нужен качественный товар.
Постепенно мы учились и рассказывали покупателю, почему важно использовать качественные дорогие маски. Несколько лет рассказывали, а потом пошли продажи. Покупатель, уже знакомый с нашей продукцией, просто решает попробовать другую линейку, понять, чем они отличается, почему такая цена. Пробует и остается доволен. Опять же наша премиум-маска Latio — не прорывная инновация. Медицинская маска изобретена уже давно, спрос на нее есть. Просто мы предложили рынку высокое качество и инновационные свойства. Как правило, из 10 абсолютно новых вещей выстреливает максимум одна, поэтому нужно привязывать инновации к продукту, понятному потребителю.
Надо ли предлагать клиентам широкий ассортимент?
На рынок мы сразу выпускаем целую линейку, а не одну маску. Сегодня в нашем ассортименте более 50 наименований: какие-то начали продаваться сразу, какие-то через год-два. Естественно, нужно постоянно быть на связи с покупателем, слышать обратную связь от рынка: где-то менять фасовку, где-то вводить новую упаковку, где-то корректировать цену. Не бывает так, что ты вбросил свой продукт на рынок и его сразу начали скупать, надо постоянно держать руку на пульсе.
В эконом-сегменте проще: два вида маски, два вида упаковки. В премиум-сегменте больше тонкостей — тут нужно поддерживать широкий ассортимент. Есть ходовые товары, которые хорошо продаются, есть те, что раскупаются хуже, но их нужно все равно держать. Например, противожидкостные маски. Когда врачи стоят на операции, если идет выброс жидкости — крови, например, а они не могут поменять маску, она должна их защитить от проникновения данной жидкости. Это специализированные маски: здесь небольшой спрос, небольшой рынок, но и они продаются.
Павел Спичаков, основатель, управляющий партнер ООО «РаСвет», ООО «КИТ», ООО «Бергус», бренды TOREX, ЛАТIО, Леля, победитель национального конкурса «Бизнес-успех» в номинации «Лучший проект в производственной сфере», председатель Союза малых промышленников, Член Совета ВО «ОПОРА РОССИИ».
Не пропустите новые публикации
Подпишитесь на рассылку, и мы поможем вам разобраться в требованиях законодательства, подскажем, что делать в спорных ситуациях, и научим больше зарабатывать.